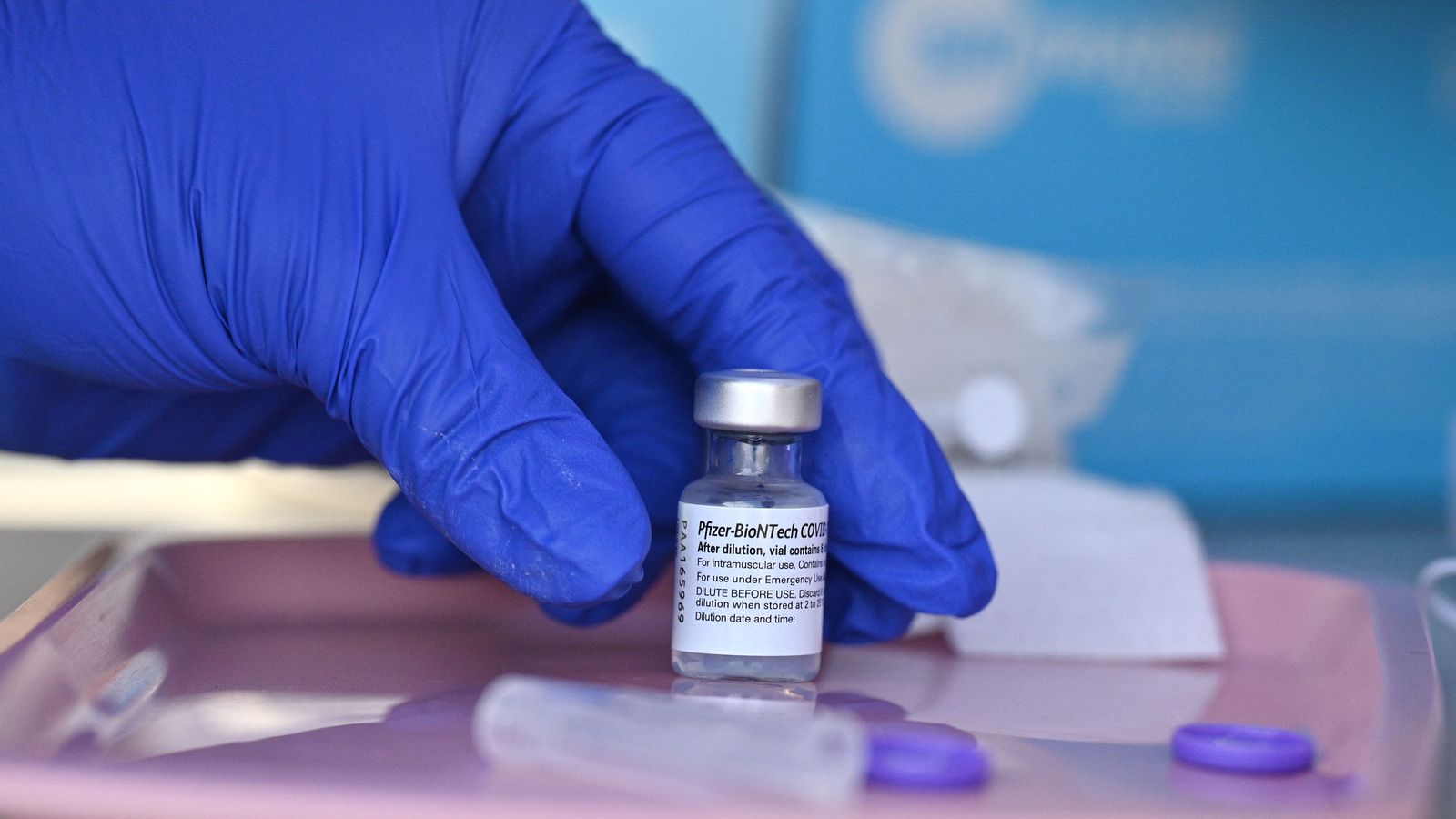
PASTILLA IN COMING. Podría ser la primera en aprobarse, al menos en EE.UU.
La farmacéutica ha detenido el ensayo clínico que estaba realizando por los buenos resultados y solicitará la aprobación del uso de emergencia.
"No podríamos estar más emocionados con los resultados", ha enfatizado Davis. "No tienes que ir al hospital, no tienes que ir a un centro para que te lo infundan. Es una píldora que se puede tomar en casa".
La compañía farmacéutica Merck, Sharp & Dome (MSD) ha anunciado este viernes que la píldora experimental que desarrolla contra la Covid-19, molnupiravir, reduce el riesgo de hospitalización y muerte a la mitad, según los datos de un ensayo clínico que se encuentra realizando. De hecho, un equipo de expertos independientes que ha supervisado el ensayo recomendó que se detuviera antes de tiempo debido a los resultados positivos obtenidos en el mismo, según informa el Washington Post.
Dado que el molnupiravir no se dirige a la proteína de la espiga del virus -el objetivo de todas las vacunas actuales contra el Covid-19-, que define las diferencias entre las variantes, el fármaco debería ser igualmente eficaz a medida que el virus siga evolucionando, según Jay Grobler, jefe de enfermedades infecciosas y vacunas de MSD.
El molnupiravir se dirige a la polimerasa viral, una enzima necesaria para que el virus haga copias de sí mismo. Está diseñado para actuar introduciendo errores en el código genético del virus. Los datos muestran que el fármaco es más eficaz cuando se administra en las primeras fases de la infección, según MSD.
Molnupiravir redujo el riesgo de hospitalización y/o muerte en todos los subgrupos clave; la eficacia no se vio afectada por el momento de inicio de los síntomas o el factor de riesgo subyacente. Además, basándose en los participantes con datos de secuenciación viral disponibles (aproximadamente el 40 por ciento de los participantes),
molnupiravir demostró una eficacia consistente contra las variantes Gamma, Delta y Mu.
La incidencia de cualquier acontecimiento adverso fue comparable en los grupos de molnupiravir y placebo (35 por ciento y 40 por ciento, respectivamente). Del mismo modo, la incidencia de acontecimientos adversos relacionados con el fármaco también fue comparable (12 por ciento y 11 por ciento, respectivamente). En el grupo de molnupiravir hubo menos sujetos que interrumpieron el tratamiento del estudio debido a un acontecimiento adverso (1,3 por ciento) en comparación con el grupo de placebo (3,4 por ciento).
El molnupiravir, administrado por vía oral, es un potente ribonucleósido análogo que inhibe la replicación del SARS-CoV-2, el virus causante de la COVID-19.
El fármaco se inventó en Drug Innovations at Emory (DRIVE), una empresa de biotecnología sin ánimo de lucro propiedad al cien por cien de la Universidad de Emory (Estados Unidos), y está siendo desarrollado por Merck en colaboración con Ridgeback Biotherapeutics.


 Al respecto, estos medios serios se han estado burlando desde hace días de la "conferencia de prensa"
Al respecto, estos medios serios se han estado burlando desde hace días de la "conferencia de prensa"